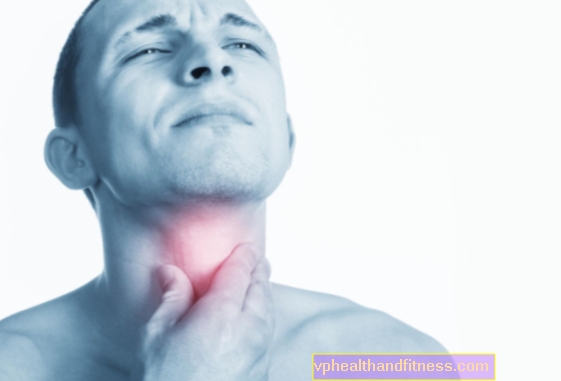
Наповнений одноразовий шприц містить 1,65 мг пегаптанібу натрію, що відповідає 0,3 мг вільного кислотного олігонуклеотиду, в номінальному обсязі 90 мкл.
| Ім'я | Зміст упаковки | Діюча речовина | Ціна 100% | Востаннє змінено |
| Макуген | 1 шт., Розчин для шоку | Пегаптаніб натрію | 2019-04-05 |
Дія
Пегаптаніб - це модифікований пегільований олігонуклеотид, який вибірково і сильно зв’язується з позаклітинною формою ендотеліального фактора росту (VEGF165), пригнічуючи його активність. VEGF - секретується білок, який індукує ангіогенез, підвищує проникність судин і є прозапальним; всі ці дії, мабуть, пояснюють прогресування ВМД з ангіогенезом. VEGF165 - це ізоформа VEGF, яка переважно бере участь у патологічних судинних новоутвореннях в очному яблуці. У пацієнтів з ВМД, які отримували пегаптаніб, спостерігали зменшення середнього розміру ураження, розміру хореоїдної неоваскуляризації (CNV) та розміру витоку флуоресцеїну. У тварин пегаптаніб повільно всмоктується з ока в системний кровотік після інтравітреального введення. Середній видимий ± період напіввиведення пегаптанібу в плазмі після дози 3 мг на одне око (у 10 разів перевищує рекомендовану дозу) становить 10 ± 4 дні. Середні максимальні концентрації в плазмі досягаються через 1-4 дні після дози 3 мг на одне око. Пегаптаніб не накопичується в плазмі після інтравітреального введення кожні 6 тижнів.Пегаптаніб метаболізується ендо- та екзонуклеазою. Виводиться з батьківською формою, а метаболіти - головним чином із сечею.
Дозування
Препарат слід застосовувати офтальмологам, які мають досвід введення інтравітреальних ін’єкцій. Препарат слід вводити раз на 6 тижнів (9 ін’єкцій на рік) у склоподібне тіло ураженого ока. Перед введенням переконайтесь, що розчин не помутнів та не змінив колір. Ін’єкції слід робити в асептичних умовах із застосуванням хірургічного миття та дезінфекції рук, стерильних рукавичок, стерильних портьєр та окуляра, а також можливості парацентезу в стерильних умовах (за необхідності). Перед ін’єкцією слід ретельно переглянути анамнез пацієнта на наявність реакцій гіперчутливості. Перед ін’єкцією слід ввести адекватну анестезію та місцевий антибіотик широкого спектру дії. Після введення препарату спостерігалося тимчасове підвищення внутрішньоочного тиску, тому слід контролювати перфузію зорового нерва та внутрішньоочний тиск. Крім того, протягом 2 тижнів після ін’єкції пацієнти повинні ретельно контролюватися на предмет кровотечі у склоподібне тіло та ендофтальміту. Якщо після 2 ін'єкцій підряд терапевтична користь для пацієнта не спостерігається (менше 15 літер, втрачених у тесті на гостроту зору) під час 12-тижневого відвідування лікування, слід розглянути питання про припинення або переривання лікування. Попередньо наповнений шприц містить надлишок препарату. Не можна вводити надмірний об’єм препарату. Надлишок слід відкинути під час підготовки до процедури введення. Немає спеціальних рекомендацій щодо застосування препарату пацієнтам літнього віку, з печінковою недостатністю або з помірною або легкою нирковою недостатністю.
Показання
Неоваскулярна (мокра) форма вікової дегенерації жовтої плями (ВМД) у дорослих пацієнтів.
Протипоказання
Підвищена чутливість до пегаптанібу або будь-якої з допоміжних речовин. Підозра або активне зараження очного яблука або його околиць.
Запобіжні заходи
Як і у випадку з іншими інтравітреальними препаратами, може спостерігатися тимчасове підвищення внутрішньоочного тиску. З цієї причини слід перевірити кровопостачання зорового нерва, а будь-яке підвищення внутрішньоочного тиску після ін’єкції слід коригувати відповідним лікуванням. Після ін’єкції пегаптанібу можуть виникати негайні (у день ін’єкції) або інтравітреальні кровотечі із затримкою. Процедура інтравітреального введення несе ризик внутрішнього запалення очей. Профіль безпеки та ефективності препарату у пацієнтів віком до 18 років не встановлений. Препарат не вивчався у пацієнтів з печінковою недостатністю або з важкою нирковою недостатністю. Введення загального обсягу попередньо заповненого шприца може призвести до серйозних побічних ефектів, тому будь-який надлишок слід видалити перед ін’єкцією.
Небажана активність
Дуже часто: запалення передньої камери, біль в очах, підвищення внутрішньоочного тиску, точковий кератит, опади та хмарність склоподібного тіла. Часто: головний біль, дискомфорт в очах, катаракта, крововилив в кон’юнктиву, гіперемія кон’юнктиви, набряк кон’юнктиви, кон’юнктивіт, дистрофія рогівки, дефект епітелію рогівки, розлад епітелію рогівки, набряк рогівки, сухість очей, запалення очей, очні виділення, запалення очей, подразнення очей, свербіж очей, почервоніння ока, набряк очей, набряк повік, посилене сльозотеча, дегенерація жовтої плями, розширення зіниці, дискомфорт в очах, очна гіпертензія, періокулярна гематома, світлобоязнь, спалахи очей, крововиливи в сітківку, затуманення зору, порушення гостроти зору, порушення зору, відшарування склоподібного тіла, порушення склоподібного тіла, нежить.Нечасто: кошмари, депресія, астенопія, блефарит, алергічний кон'юнктивіт, відкладення на рогівці, крововилив в очі, свербіж повік, кератит, крововилив у склоподібне тіло, порушення рефлексів зіниць, потертість рогівки, ексудат сітківки, звисання століття, рубець сітківка, халязіон, виразка рогівки, зниження внутрішньоочного тиску, реакція на місці ін’єкції, утворення бульбашок на місці ін’єкції, відшарування сітківки, розлад рогівки, закриття артерії сітківки, розрив сітківки, ектропія, ненормальний рух очей, подразнення століття, крововилив у передню камеру , розлад зіниць, розлад райдужки, пожовтіння ока, увеїт, відкладення на задній частині ока, ірит, ямка на зоровому нерві, деформація зіниць, закриття вен сітківки та випадання склоподібного тіла, глухота, загострення хвороби Меньєра, запаморочення, серцебиття серце, високий кров'яний тиск, аневризма аорти, запалення біль у горлі, блювота, розлад травлення, контактний дерматит, екзема, зміна кольору волосся, висип, свербіж, нічна пітливість, біль у спині, втома, озноб, болючість, біль у грудях, грипоподібні симптоми, підвищений рівень GGT, стирання. Невідомо: анафілактична реакція (включаючи набряк Квінке). У постмаркетинговому досвіді повідомлялося про рідкісні випадки анафілактичних / анафілактоїдних реакцій, включаючи ангіоневротичний набряк, у пацієнтів протягом декількох годин після прийому пегаптанібу та інших лікарських засобів, що вводились під час процедури підготовки до ін’єкції. Через неможливість видалити надлишковий об’єм продукту із попередньо наповненого шприца перед ін’єкцією, повідомлялося про випадки сильного підвищення внутрішньоочного тиску, що вимагало пункції передньої камери ока. Також спостерігалося стійке незначне підвищення внутрішньоочного тиску після багаторазових інтравітреальних доз у постмаркетинговому спостережному дослідженні. Ймовірність підвищеного внутрішньоочного тиску була в 1,128 рази при кожній наступній інтравітреальній ін’єкції (р = 0,0003). Статистично значущих відмінностей у частоті підвищеного внутрішньоочного тиску між пацієнтами з підвищеним внутрішньоочним тиском або глаукомою в анамнезі та пацієнтами без анамнезу не було.
Вагітність і лактація
Пегаптаніб не вивчався у вагітних. Дослідження на тваринах недостатні, але показали токсичний вплив на репродуктивну функцію при високих дозах та системному впливі. Системний вплив після внутрішньоочного введення, ймовірно, буде дуже низьким. Препарат слід застосовувати під час вагітності, лише якщо потенційна користь для матері виправдовує можливий ризик для плода. Невідомо, чи препарат виводиться з молоком - не рекомендується застосовувати препарат під час годування груддю.
Коментарі
У пацієнтів може спостерігатися тимчасове погіршення гостроти зору після інтравітреального введення; поки ці симптоми не зникнуть, не слід керувати автотранспортом або працювати на машинах. Зберігати в холодильнику (2-8 градусів С); не заморожувати.
Взаємодія
Досліджень лікарських взаємодій не проводилося. Пегаптаніб метаболізується нуклеазою, тому не слід очікувати взаємодій, пов’язаних із системою цитохрому Р450. Два дослідження на ранніх стадіях, проведені у пацієнтів, які отримували лише рецептуру або рецептуру та фотодинамічну терапію, не показали явних відмінностей у фармакокінетиці пегаптанібу у плазмі крові.
Препарат містить речовину: Пегаптаніб натрію
Відшкодований препарат: НІ






zapalne-w-wyrostkach-sutkowatych-k-skroniowej-porada-eksperta.jpg)